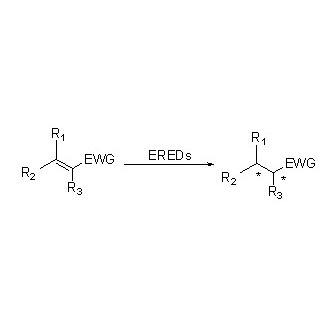
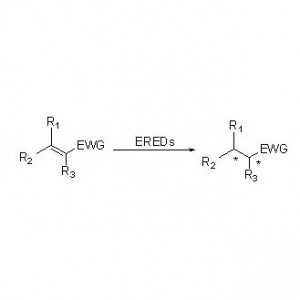
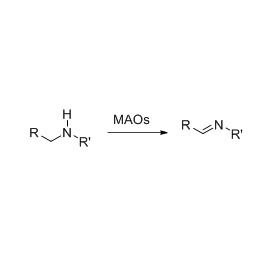
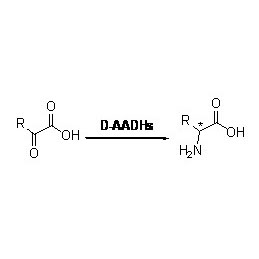
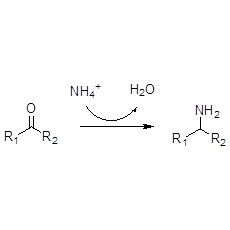
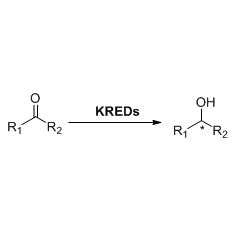
Ene reduttasi (ERED)
Gli ES-ERED catalizzano vari tipi di substrati grazie al loro ampio spettro. In generale, i legami C=C dei composti α,β-insaturi con gruppi elettron-attrattori (tra cui chetoni, aldeidi, gruppi nitro, acidi carbossilici, esteri, anidridi, lattoni, immine, ecc.) vengono facilmente ridotti dagli ES-ERED, mentre i doppi legami non attivati non lo sono.
Esistono 46 tipi di prodotti enzimatici ERED (numerati da ES-ERED-101 a ES-ERED-146) sviluppati da SyncoZymes.
Meccanismo catalitico:
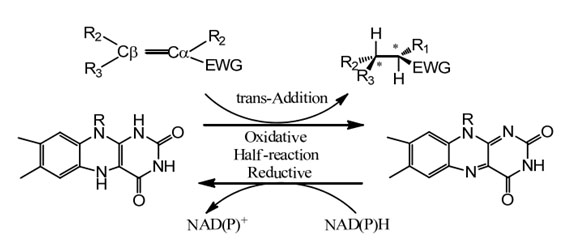
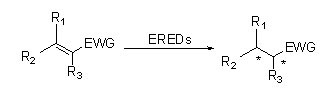
| Enzimi | Codice prodotto | Specifiche |
| Polvere enzimatica | ES-ERED-101~ ES-ERED-146 | un set di 46 Ene Reduttasi, 50 mg ciascuna 46 articoli * 50 mg / articolo, o altra quantità |
| Kit di screening (SynKit) | ES-ERED-4600 | un set di 46 Ene Reduttasi, 50 mg ciascuna 46 articoli * 50 mg / articolo, o altra quantità |
★ Elevata specificità del substrato.
★ Elevata selettività chirale.
★ Elevato tasso di conversione.
★ Meno sottoprodotti.
★ Condizioni di reazione lievi.
★ Rispettoso dell'ambiente.
★ Elevata sicurezza.
➢ Normalmente, il sistema di reazione dovrebbe includere substrato, soluzione tampone (pH di reazione ottimale), coenzimi (NAD(H) o NADP(H)), sistema di rigenerazione dei coenzimi (ad esempio glucosio e glucosio deidrogenasi) ed ES-ERED.
➢ Tutti gli ES-ERED possono essere testati rispettivamente nel sistema di reazione sopra descritto o con il kit di screening ERED (SynKit ERED).
➢ Tutti i tipi di ES-ERED corrispondenti alle varie condizioni di reazione ottimali dovrebbero essere studiati individualmente.
➢ Un substrato o un prodotto ad alta concentrazione può inibire l'attività di ES-ERED. Tuttavia, l'inibizione può essere alleviata mediante l'aggiunta di substrato in batch.
Esempio 1 (aldeidi o chetoni α,β-insaturi)(1):
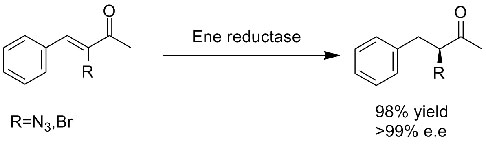
Esempio 2 (acidi carbossilici α,β-insaturi e loro derivati)(2):
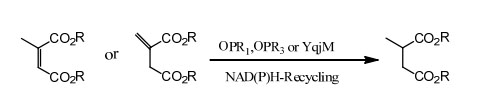
Conservare a una temperatura inferiore a -20℃ per 2 anni.
Evitare il contatto con condizioni estreme quali: temperature elevate, pH elevato/basso e solventi organici ad alta concentrazione.
1. Lucidio C, Fardelone J, Augusto R, e tal. J.Mol.Catal.B:Enzym., 2004, 29: 41-45.
2. Stueckler C, Hall M, Ehammer H, e tal. .Org.Lett, 2007, 9(26): 5409-5411.